ノイシリン、ノイシリンAは優れた制酸剤として国内外で既に高く評価され、胃腸薬製剤の原料として大量に使用されております。その卓越した医療効果は、酸中和能が大きく、即効性であり、またpH3~5を長時間持続する特徴と、抗ペプシン作用を有し胃粘膜を被覆保護する性質によるものとなります。ここでは、ノイシリン、ノイシリンAの制酸剤として利用に焦点を当てて紹介します。
fa-envelope-o
ノイシリン・ノイシリンAの薬理試験
ノイシリン(メタケイ酸アルミン酸マグネシウム)およびノイシリンA(ケイ酸アルミン酸マグネシウム)は非吸収性で、試験管内試験(Fuchs法)において適切な胃液pHを長く保ち、経時変化なく臨床薬理試験(Katsh-Kalk法)においてもほぼ全例で胃液酸度を低下させる。
また、抗ペプシン作用、胃粘膜保護作用を有しているため抗潰瘍実験(幽門結紮法)では明らかな抑制効果が認められる。他方、ノイシリンおよびノイシリンAは炭酸水素ナトリウムのようなアルカロージスは認められていない。
また、アスピリンやスルファニルアミドと併用投与しても、それぞれの吸収に影響を与えず、各種の消化酵素にノイシリンを配合した場合でもAmylase活性、Protease活性を阻害することはない。
制酸力試験
ノイシリンおよびノイシリンAの制酸力は1g当り0.1N-塩酸でそれぞれ200mlおよび250ml以上である。
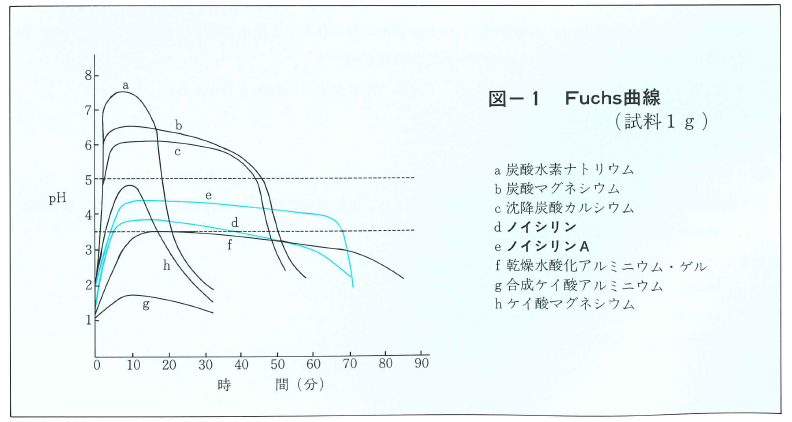
Fuchs法または同変法を用いてノイシリンの制酸力を調べたところ、ノイシリンの1gはこれらの胃模型内において、0.1N-塩酸を速やかにpH3以上に中和し、50~60分以上にわたりpH3~5に保つ。各種制酸剤のFuchs曲線を図‐1に示す。
各種制酸剤のFuchs曲線
臨床 薬理試験
種々の疾患患者にKatsh-Kalk法による胃液検査を行う際、ノイシリン又はノイシリンAを投与し、その前後の胃液酸度を比較する実験がいくつか行われている。
それによると、ほとんど全例に酸度の低下が認められ、ヒスタミン刺激による胃液検査法を用いてノイシリン投与前後の酸度を比較した実験では7例中5例に顕著な低下、1例に中程度の低下を認めている。
また、ノイシリン1g服用後ラジオカプセルにより胃内pHを測定したところ、明らかにpHの上昇が認められている。
臨床試験1 胃液酸度ならびにペプシン作用に及ぼす影響について
胃液酸度測定:
Katsh-Kalk「カフェイン」法で10分間隔で2時間、胃液を採取し測定。
ペプシン活性測定:
Gruetzner氏法に従い試験液投与前後および1,2時間後に測定。
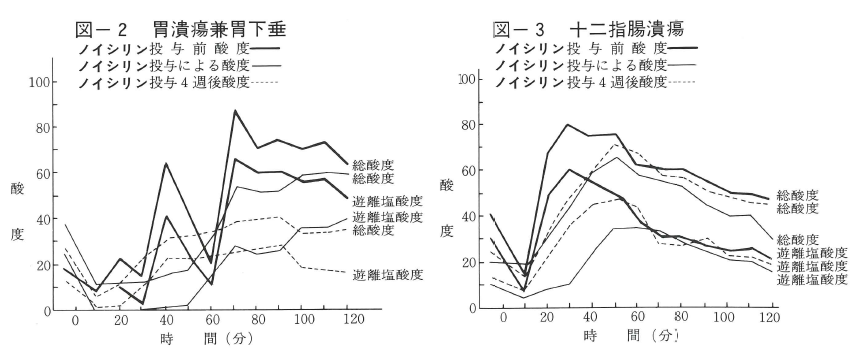
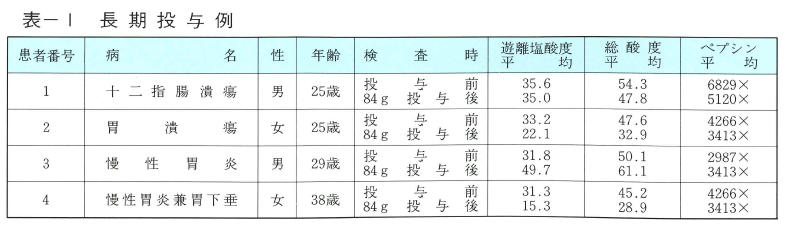
2例について①ノイシリン投与前の酸度およびペプシン作用、②ノイシリン投与による酸度およびペプシン活性-カフェイン液にノイシリン1gを混じて投与し胃液採取、③ノイシリン投与(1日3g食間服用)4週間連続投与後の酸度およびペプシン活性を測定した結果を図‐2,3,また長期投与による胃液酸度およびペプシン活性の変化を表-1に示す。
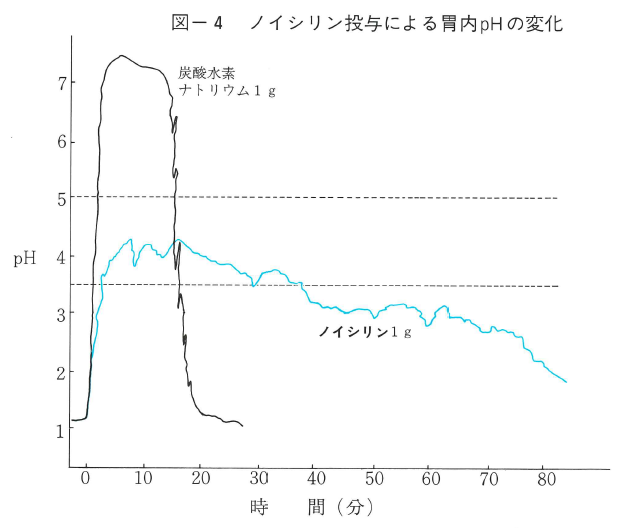
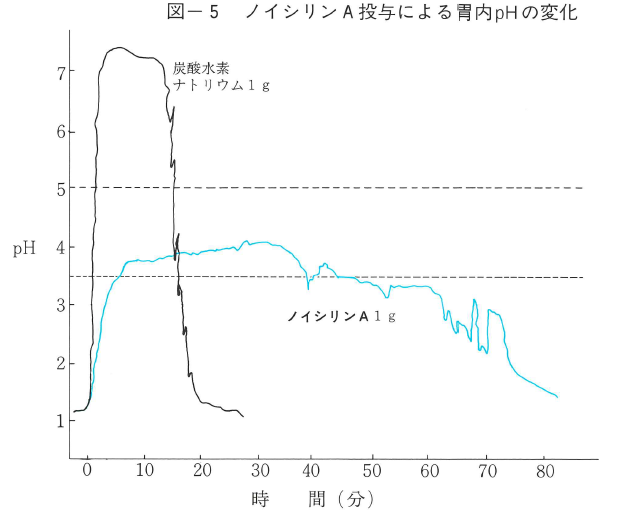
臨床試験2 ラジオカプセルによる胃内pHの測定
図-4,5はノイシリン、ノイシリンA投与による胃内pHの変化を、ラジオカプセルによって測定した結果である。炭酸水素ナトリウムに比較して極めて長時間、酸中和作用が持続していることが認められる。
胃粘膜保護作用
硫酸バリウムとノイシリンの混合投与によるX線撮影を行って、バリウムの胃内滞留時間を、バリウム単独の場合と比較したところ、ノイシリン混合の場合の方が長く滞留することを認め、その結果からノイシリンの胃粘膜保護作用が推定された。
また、胃炎患者の胃液に各種制酸剤を混合したところ、炭酸水素ナトリウムの場合は粘液を溶解するが、ノイシリンの場合は粘液を吸着して膠状沈殿を作り白濁することが認められ、この沈殿物が胃粘膜保護作用を発揮するものと思われる。
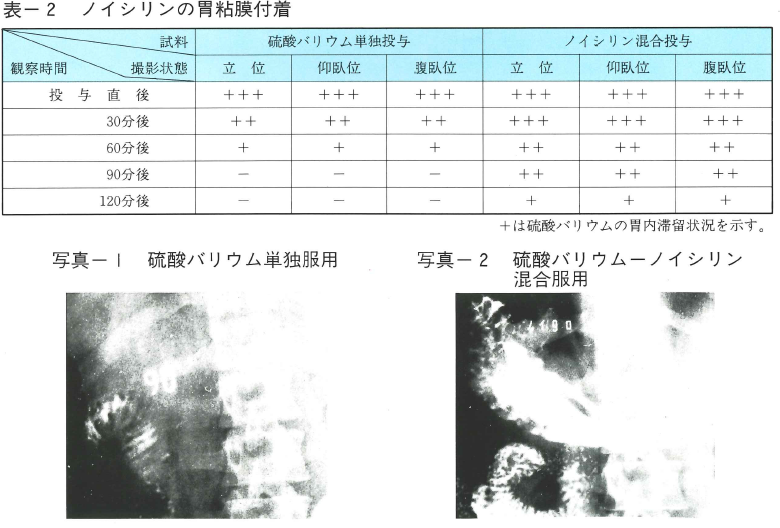
臨床試験1 硫酸バリウムの胃内滞留に及ぼす影響について12)
硫酸バリウム50gを水100mlに懸濁した試料およびその中にノイシリン1gを添加した懸濁剤を服用後30~120分にわたってX線撮影を行った。
胃粘膜付着状況は表-2の通りで硫酸バリウム単独投与とノイシリン混合投与を比較すると、胃内滞留量ならびに時間に有意差が認められた。写真‐1,2は90分後の状態を示す。
臨床試験2 各種制酸剤の胃粘膜に及ぼす影響
胃炎患者の胃液5mlに各種制酸剤0.1gずつ加え振盪し、38.0℃、2時間放置後胃粘液の溶解性を検しながら直径4.5㎝の皺襞ろ紙を用いてろ過し、その時間を測定した。
粘液を溶解して透明となり、ろ過時間も短縮、残渣少量。酸化マグネシウム:
混和振盪により白濁するが上清は不透明。ろ過時間変わらず、残渣多量。ノイシリン:
混和振盪により著明に白濁し、放置すると上清は澄明、ろ過時間やや短縮。
以上のごとく、ノイシリンは胃液に溶解せず、粘液も溶解しないが、粘液を吸着し膠状沈殿物を作るので胃粘膜の保護作用が考えられる。
実験潰瘍抑制作用
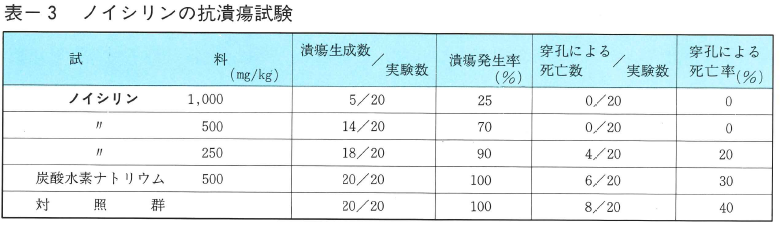
試験1 抗潰瘍試験
Shayらの方法(1945)を用いてWister系雄性ラットにノイシリンを経口投与して実験潰瘍抑制試験を行った。その結果、抗潰瘍作用において、ノイシリン500、1,000㎎/㎏投与群で炭酸水素ナトリウム500㎎/㎏投与群および対象群との間に明らかな差が認められた。
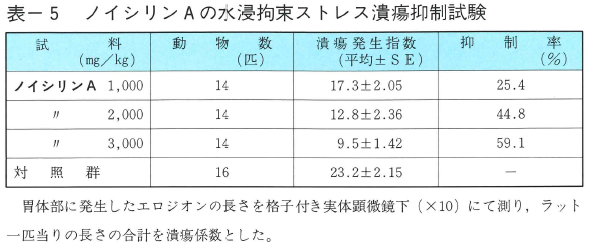
試験2 ストレス潰瘍抑制試験
高木らの方法(1568)を用いて、Donryu系ラットにノイシリンAを経口投与して水浸拘束ストレス潰瘍抑制試験を行った。その結果2,000~3,000㎎/㎏投与群では対象群と比較し、顕著な抗潰瘍作用が認められた。
試験3 ヒスタミン潰瘍抑制試験
Eagletonらの方法(1971)を用いて、Hartley系白色モルモットにノイシリンAを経口投与して、ヒスタミン潰瘍抑制試験を行った。その結果、50㎎/㎏投与群で対象群と比較し、顕著な抗潰瘍作用を認められた。
薬剤 の吸収に及ぼす影響
アスピリンの吸収に及ぼす影響
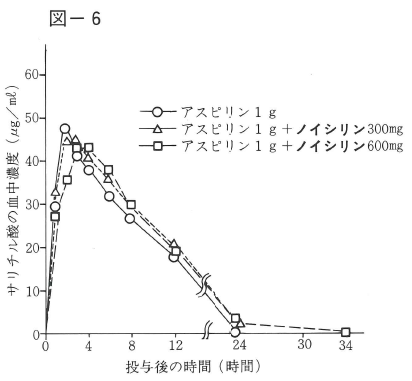
22~30歳の健康男子5名に、主役としてアスピリン1g単独又はノイシリン300㎎あるいは600㎎との同時投与をクロス・オーバー法にて行った。採決は投与後一定時間に行い、尿は34時間後までの全尿を合し、それぞれサリチル酸として血中及び尿中への排泄量の測定を行った。
この結果、アスピリンの血中濃度及び尿中への排泄量にはノイシリンの同時投与による影響は認められなかった。従ってノイシリンは酸性薬物であるアスピリンの消化管からの吸収には影響しないことが明らかとなった。
スルファニルアミドの吸収に及ぼす影響
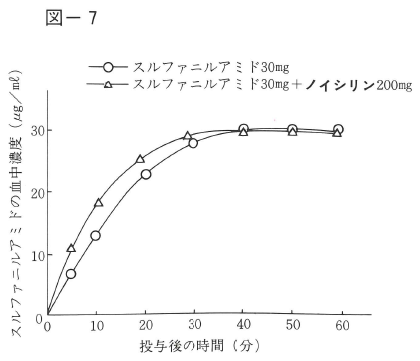
Wistar系雄性ラット(体重170~190kg)を用い、0.6%スルファニルアミド水溶液5mlにノイシリン200㎎を懸濁させたものをゾンデにて経口投与した。
投与後、尾部より経時的に採血し、常法によりサルファ剤の血中濃度を測定した。その結果、投与20~30分後にスルファニルアミドは最高血中濃度に達した。
ノイシリン添加の場合と、添加しない場合とを比較すると、最高濃度値、その到達時間、ならびに血中濃度上昇パターンのいずれにも有意な差は認められなかった。
テトラサイクリンなどの吸収に及ぼす影響
重炭酸ナトリウム、アルミニウム、カルシウム、マグネシウムを含む制酸剤は、テトラサイクリンの吸収を阻害するという文献がある。然し、このような場合テトラサイクリン投与後30~60分してノイシリンを投与すれば改善される。
デンプン、蛋白消化に及ぼす影響
可溶性デンプン及び酸変性ヘモグロビンからなる胃膜型を用い、制酸剤によるジアスターゼ、タカジアスターゼとパンクレアチンのデンプン・蛋白消化力に及ぼす影響を調べた。
ノイシリンを添加した場合、酵素剤を単独で使用した対象群と比較して、ジアスターゼのデンプン消化力と、パンクレアチンの蛋白消化力は著しく増加したが、タカジアスターゼのデンプン及び蛋白消化力、また、パンクレアチンのデンプン消化力には影響を及ぼさなかった。
酵素剤と制酸剤を配合した場合の酵素活性測定について
酵素剤としてビオジアスターゼ500、プロザイム、リパーゼを、制酸剤としてノイシリンをそれぞれ1:10の割合で配合し、酵素剤単独の活性を100とした時のpHによる相対活性を求めた。
アミラーゼ(pH5.0)
〔酵素剤〕ビオジアスターゼ